طراحی الکترولیتی برای باتری های لیتیومی بدون کبالت با آند سیلیسیم دی اکسید
تاریخ انتشار روی سایت: 19 بهمن ماه 1402
تاریخ انتشار بر روی ژورنال: 27 مهر ماه 1402
نویسندگان: Seongjae Ko, Xiao Han, Tatau Shimada, Norio Takenaka, Yuki Yamada & Atsuo Yamada
DOI: https://doi.org/10.1038/s41893-023-01237-y
نگارشگر خلاصه نامه: سید امیرحسین میرصدری
همه ما با باتري هاي پايه ليتيومي آشنا هستيم و حتي حداق كبار تجربه استفاده از آن ها را نيز داشته ايم. اين باتري ها میتوانند با قیمت معقولی، ظزفیت و توان خوبی از خود نشان دهند در حالی که گروهی از آنها میتواندد از مواد زیست سازگار ساخته شوند. این باتری ها عموما دارای آندی از جنس کربن و یا گرافیت، کاتدی از جنس اکسید فلزاتی که لیتیم نیز درون آن آلیاژ شده و الکترولیتی از جنس مواد آلی که میتوانند یون های لیتیم را درون خود حفظ کنند. اما بسیاری از این باتری ها از کبالت در ساختار کاتدی خود بهره میبرند. متاسفانه عنصر کبالت در روی زمین از معادن بسیار کمی برخوردار است و به اینصورت هستش که تنها در کشور کنگو یافت میشه و از مشکلات عدیده این معادن، استفاده از بچه های کار در این گونه معادن هست. در این مقاله بجای استفاده از آند گرافیتی، از SiOx و در کاتد بجای LiCoO2 از LiNi0.5Mn1.5O4 استفاده شده است. این ترکیب بدلیل پایداری و همچنین پتانسیل بیشتر نسبت لیتیم مورد توجه هستش ولی موضوع اصلی این هستش که الکترولیتی که برای این سیستم میتوانستیم استفاده کنیم در پتانسیل های بالا قدرت پایداری ندارند و تجزیه میشوند. علاوه بر این مشکل عدیده ای که برای این سیستم پیش می آید آسیب دیدن و خورده شدن الکترودها در پتانسیل های بالا هست.
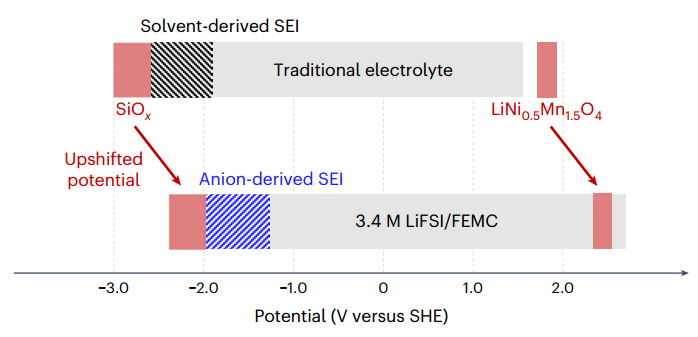
این اتفاقات تماما وابسته به واکنش ها و پتانسل شیمیایی لیتیم با یون لیتیم است که در الکترولت اتفاق می افتد. برای حل این مشکلات و همچنین حفظ ظرفیت بالقوه و عملی 4/7 ولتی باتری توصیف شده، باید سیستمی با الکترولیتی مناسب طراحی کنیم که بتواند پایداری خود را در محدوده احیایی ماکزیمم حفظ نماید و تجزیه نشود که این تجزیه نیز باعث خوردگی الکترود شود (چون پتانسیل تبدیل یونی لیتیم از محدوده پتانسیل سیلیسیم اکسید و لیتیم نیکل منگنز اکسید خارج است). از اینرو از الکترولیت های عامل دار شده و یا الکترولیت هایی که فیلم غیرفعالساز (Passivation) روی الکترود ایجاد میکنند استفاده میشود. بطور مثال میتوان به الکترولیت هایی مثل 1 و 2 دی متوکسی اتان تترا هیدرو فوران و یا آنهایی که دارای فلوئور هستند مانند فلوئورو اتیلن کربنات. برای ایجاد مقاومت در پتانسیل های احیایی بالا باید بتوان کاری کرد تا پتانسیل الکترولیت را نسبت به الکترود شیفت مثبت داد و این گروه تحقیقاتی به این نتیجه رسیده بودند که پتانسیل شیمیایی تبدیل لیتیوم به یونش که دلیل شیفت مثبت پتانسیل بود میتواند توسط ایجاد ساختارهای به هم پیوسته یونها (Li-Li , Li-ion) ایجاد شود. برای این مهم، الکترولیتی برپایه لیتیم نیتروژن گوگرد دی اکسید دی فلوئورینات/ متیل (2.2.2 تری فلئورو اتیل) کربنات استفاده شد. برای متوجه شدن عامل ایجاد ساختار یون-یون، محاسبات شبیه سازی کامپیوتری با نرم افزار گوسین 16 انجام شد و دانشمندان متوجه شدند که افزایش غلظت میتواند بر ایجاد این نوع ساختارها تاثیر گزارد که بیشترین غلظت (3/4 مولار) بهینه ترین حالت الکترولیت بود. برای اینکه متوجه شوند که کدام الکترولیت انتخابی از سه الکترولیت مختلف طراحی شده میتواند مقاومت احیایی داشته باشد، از 80 سیکل کند شارژ دشارژ استفاده شد که با 150 میلی آمپر بر هر گرم جریان ثابت که سه ماه طول کشید، استفاده شد و الکترولیت 3/4 مولار لیتیم نیتروژن گوگرد دی اکسید دی فلوئورینات/متیل (2.2.2 تری فلئورو اتیل) کربنات از همه بیشتر ظرفیت بهتری در واحد درصد از خود به نمایش گزارد.
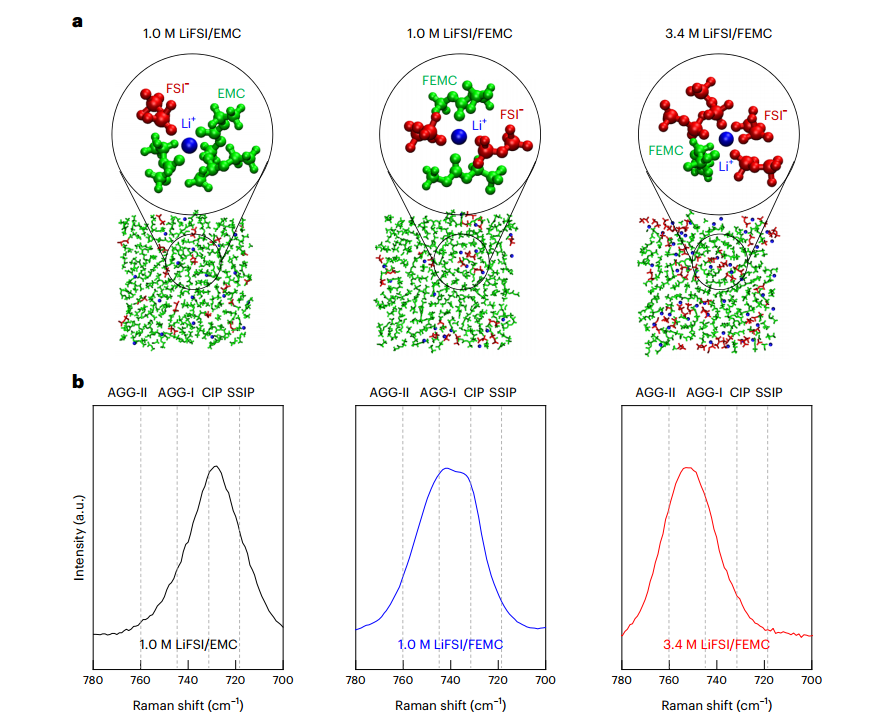
توسط آزمایشات ولتامتری چرخه ای مشخص شد که پتانسیل احیایی الکترولیت با افزایش مقدار غلظت و همچنین الکترولیت توصیف شده در پتانسیل های بالاتری شیفت پیدا کرده است. پایداری در سیکل های اکسیدی هم بخاطر وجود یون های الکترون دهنده فلئور بصورت پایداری ثابت باقی میماند. خوردگی فلزاتی همچون آلومینیوم زمانی رخ میدهد که آلومینیوم بصورت 3+Al در داخل الکترولیت نفوذ کند. این اتفاق در این الکترولیت بهینه کمتر اتفاق می افتد بدلیل اینکه حل کنند این الکترولیت بسیار کمتر است و همچنین ظرفیت ایجاد ساختار جفت یون در این الکترولیت برای عنصرهایی مانند آلومینیوم و مس بسیار پایین است (در این مقاله سیلیسیم اکسید و کاتد روی مس و آلومینیوم قرار گرفته اند). الکترود ها همگی از نمکت لیتیم ساخته شده و الکترولیت هم بصورت تجاری خریده شده بودند و از دستگاه هایی همچون XPS، EDX، گالوانواستات و پتانسیواستات برای آزمایشات ظرفیت باتری و امپدانس استفاده شد. همچنین این سیستم در یک سل سکه مانند 2032 طراحی شد و از سلولز و پلی پروپیلن و پشم شیشه به عنوان جدا کننده استفاده شده بود.
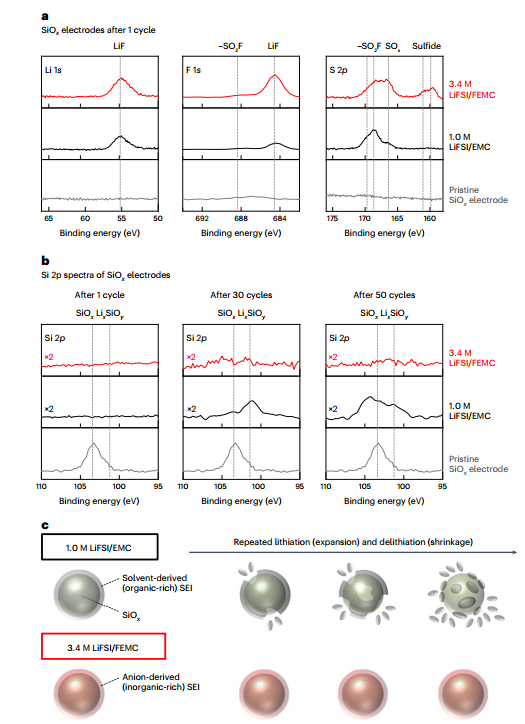


klsjuidhfasdgh.png)
klsjuidhfasdgh.png)
klsjuidhfasdgh.png)
klsjuidhfasdgh.png)
klsjuidhfasdgh.png)

klsjuidhfasdgh.png)
klsjuidhfasdgh.png)
klsjuidhfasdgh.png)